Réactions acido-basiques| Chimie terminale

I Définition acide et base
Un acide est une espèce qui peut perdre un ion H+ (= proton)
Une base est une espèce qui peut gagner un ion H+ (=proton)
On définit un couple A/B par une demi-équation acido-basique:
acide = base +H+
Exemple: CH3COOH/CH3COO-
➥CH3COOH = acide
➥CH3COO- = base
Et CH3COO- + H+ = CH3COOH
➨Une réaction acido-basique est un échange d'ion H+ (=proton) entre l'acide et la base d'un même couple
II Autoprotolyse de l'eau
1) Le produit ionique de l'eau
L'eau pure conduit très légèrement le courant, car elle contient quand même des ions
➥Dans l'eau, il y a constamment des réactions chimiques immédiates entre les molécules d'eau
2H20 ⇆ HO- + H3O+
HO-: ion hydronium
H3O+: ion oxonium
Tableau d'avancement pour cette réaction, avec 1L d'eau
Pour le tableau d'avancement de cette réaction, avec 1L d'eau on a xf ≈ 10-7 mol
Produit ionique de l'eau Ke
$ Ke = [{H_3}^{O + } ]_f ✕ [HO^-]_f = 10^{-14}$
➥Constante, marche pour une température de 25°
[X]: concentration de l'espèce X
f: valeur à l'état final
2)Définition du pH
-Le pH donne l'acidité ou la basicité d'une solution
- pH = -log [H3O+]f
➥[H3O+] = 10-pH
Avec la concentration en mol/L
Cette formule marche pour une concentration < 1mol/L
Pour avoir une solution neutre, il faut [H3O+] = [HO-]
➥Les concentrations doivent être de 10-7 (car 2 ✕ 10-7 = 10-14 = Ke)
-Une solution neutre a donc un pH de 7
REMARQUE:
Le couple de l'eau est: H20/HO- ET H30+/H2O
➥H20 est amphotère car elle est acide ET basique
Si: [H3O+] tend vers 1 mol/L
➥Le pH tend vers 0
Alors [HO-] tend vers 10-14 mol/L
➨On a une solution très acide
Si: [HO-] tend vers 1 mol/L
➥Le pH tend vers 14
Alors [H3O+] tend vers 10-14 mol/L
➨On a une solution très basique
III Constante d'acidité d'un couple acido-basique
La constante d'acidité sert à prévoir l'état final d'une réaction acido-basique
AH/A-, un couple acido-basique quelconque que l'on mélange avec de l'eau
Équation de la réaction:
AH +H20 ⇆ H3 O+ + A-
Constante d'acidité Ka:
KaAH/A = ${[H_3O^ + ]_f ✕ [A^{-}]_f}/{[AH]_f}$
Exemple
On dissout 3.10-3 mol de NH4+ dans 1L d'eau
Équation:
NH4+ + H20 ⇆ NH3 + H3O+
Note:
Couple acido-basique: NH4+/NH3
KaNH4+/NH3 = 6,3 ✕ 10-10 (coefficient d'acidité)
On cherche à calculer la concentration de toutes les espèces présentes dans la solution
Tableau d'avancement
| NH4+ + | H20 ⇆ | NH3 + | H3O+ |
|---|---|---|---|
| 3.10-3 | excès | 0 | 0 |
| 3.10-3 - xf (=0) | excès | xf | xf |
Donc: $ Ka = {[H_3O^ + ]_f ✕ [NH_3]_f}/{[NH_4 ^ + ]}$
Qui est égale à ${({xf}/V)²}/(3.10^{-3} - xf)/V = {[H_3O^+]²}/(3.10^{-3} - [H_3O^+])$
➥ car la concentration est égale à xf
➥Réaction quasi-totale
IV Classement des forces des acides et des bases
1) Définition du pKa
Le pKa donne la force de l'acide
pKa = -log(Ka)
➥ On peut en déduire: Ka = 10-pKa
Plus l'acide est fort, plus le pH tend vers 0, plus le pKa tend vers 0
➥On n'utilise pas le pKa pour les acides forts
2) Les acides forts
Un mélange entre un acide fort et de l'eau donne une réaction chimique quasi-totale
➨Comme la réaction est quasi-totale, on a xf = concentration du réactif limitant
Exemple d'acide fort:
-Acide chlorhydrique (HClg)
-Acide sulfurique (H2SO4)
-Acide nitrique (HNO3)
3)Les acides faibles
Un mélange entre un acide faible et de l'eau donne une réaction limité
La plus part des acides carboxylique sont des acides faibles
Exemple d'acide faible: CH3COOH
On peut classer les acides par le pKa en faisant un tableau
➥Plus on monte, plus le pKa est fort, plus l'acidité est faible, plus la basicité est forte
➥Plus on descend, plus le pKa est faible, plus l'acidité est forte, plus la basicité est faible
4)Les bases fortes
Dans l'eau, une base forte se transforme totalement en HO-
➥Réaction quasi-totale
Exemple de base forte:
La soude hydroxyle de sodium (Na+,HO-)
5)Les bases faibless
Dans l'eau, les bases faibless ont une réaction limitée
➥Réaction non totale
Exemples de bases faibles:
-Les amines, R-NH2 (R: une chaîne carbonée)
➥ RNH2+H2O⇆RNH3+
L'amine le plus connue et le plus simple: l'ammoniac (NH3
V diagramme de prédominance
1) Relation entre pKa et pH
Démonstration de la relation entre le pKa et le pH
[A-]: concentration de la base
[AH]: concentration de l'acide
KaAH/A = ${[H_3O^ + ]_f ✕ [A^{-}]_f}/{[AH]_f}$
➥ log Ka = log ([H3O+]f ✕ [A-]f)/[AH]f
➥ log ka = log [H3O+]f + log ($[A^{-}]_f/[AH]_f$)
➥ -log ka = -log [H3O+]f - log ($[A^{-}]_f/[AH]_f$)
Comme -log [H3O+]f = pH et-log ka = pka
On a la relation:
$ pH = pKa \; + \; log( {[A^{-}]_f}/{[AH]f})$
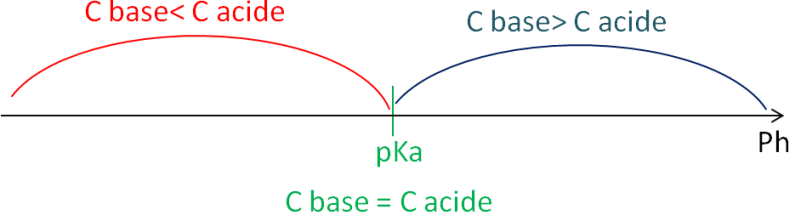
2) Diagramme de prédominance
C base = concentration de la base = [A-] (= C de A-)
C acide = concentration de l'acide = [AH] (= C de AH)
3) Cas des acides aminés
Les acides aminés ont une fonction d'acide carboxylique et d'aminé
➥Ils ont une fonction d'acide ET une fonction de base
Étant acide ou base, les aminés ont 2 pKa
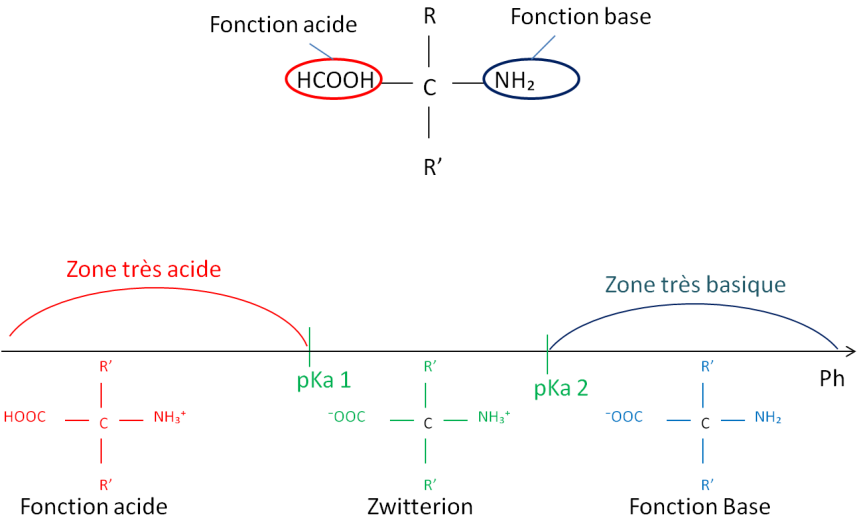
➨ Les aminé ont des charges négative (anion) pour la partie basique ( supérieur à pKa2)
➨ Les aminé ont des charges positive pour la partie acide (inférieur à pKa1)
Entre pKa1 et pKa2, on a un molécule avec une charge + ET une charge -
➥ c'est un Zwitterion
Lors d'un titrage avec des acides aminés, il y a 2 réactions simultanées
Exemple avec la glycine (AH2+)
Couples acido basique: AH2+/AH et AH/A-
Si on titre avec HO-, on a:
AH2+ +HO- → AH + H2O
ET
AH+HO- → A-+H2O
Ce qui donne la réaction: AH2+ +2HO- → 2H2O+A-
Les outils de la chimie analytique
-
Partagez ce cours !
Suivez Nicolas KRITTER sur google + ( cours inspiré de celui fait par le professeur de la classe)
