La Spectroscopie

Les molécules organiques peuvent absorber des radiations de lumière
Comme les molécules et atomes ne peuvent absorber qu'une certaine quantité d'énergie, on peu les analyser en utilisant la Spectroscopie
RAPPEL: ΔE = h ✕ f
On utilise la spectroscopie pour modifier l'emplacement des électrons sur les couches, faire vibrer les liaisons d'une molécule, créer des rotations autour des liaisons ou bien changer l'alignement des noyaux des atomes
Spectroscopie UV-visible
Les molécules organiques qui ont des doubles liaisons conjuguées peuvent absorber de la lumière visible
➥Elles sont alors colorées
On utilise donc la Spectroscopie UV-visible pour ces molécules colorées et aux molécules qui absorbent dans l'ultra-violet
➥Elles absorbent des longueurs d'onde comprises entre 200nm et 800 nm
Loi de Beer-Lambert
La loi de Beer-Lambert dit que l'absorbance est proportionelle à la concentration
On a: A = k ✕ C
On se place à la longueur d'onde où l'absorption est la plus forte pour avec un résultat plus précis lors des mesures
REMARQUE: la loi de Beer-Lambert ne s'applique que dans un certain intervalle de concentration, elle ne fonctionne plus si l'absorbance est trop forte
Spectroscopie dans le visible (400 < λ < 800)
Pour qu'une substance soit colorée, il faut qu'elle absorbe dans le domaine visible
➥La méthode est la même que pour l'étude des substances qui absorbent dans l'ultra-violet
Une substance absorbe la couleur complémentaire de sa propre couleur
Exemple: la Β-carotène (orange) absorbe dans le bleu
Spectroscopie IR
Principe
On étudie ici la zone centrale de l'infrarouge: entre 2,5 et 16 micromètre
Comme le rayonnement IR a une longueur d'onde plus grande que l'UV, le rayonnement IR fournit un quanta d'énergie plus faible
➥On ne peut donc pas provoquer de transition électronique
Lors d'une spectroscopie IR on crée alors une rotation ou une vibration des atomes de la molécule
Chaque atome qui rentre en rotation ou en vibration, a une fréquence qui lui est propre
➥A Cette fréquence correspond une bande d'absorption pour une certaine longueur d'onde
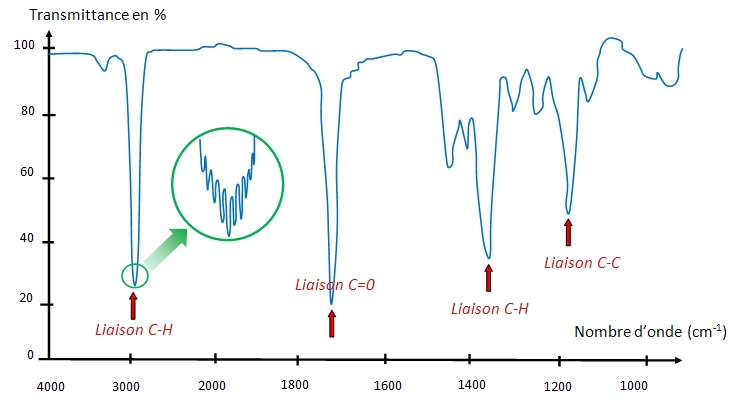
Spectre IR
Pour avoir le spectre IR, on utilise un spectromètre
Comme la plus part du temps, on mesure la transmitance T (en %), en fonction du nombre d'onde (=$1/λ$), on a des pics en négatifs
➥100% de transmitance est en Bas du graphique, 0% en haut
Il est impossible d'attribuer à chaque bande d'absorption une longueur d'onde précise car il y a un trop grand nombre de possibilité de rotation autour des liaisons
➥Les spectres IR sont très complexes à étudier
Exploitation d'un spectre IR
On utilise la spectroscopie IR pour trouver les liaisons caractéristiques dans une molécule
Pour les trouver, on utilise un tableau qui relie ces liaisons et les bandes d'absorptions
Dans l'analyse du spectre, on tient compte de l'intensité et de la forme des bandes d'absorptions
Vibrations facilement repérables sur un spectre IR
Groupement -OH
Bande large et souvent de forte intensité
Sa position et sa forme est liée à la présence de liaison hydrogène
Pic entre 3590 et 3600 cm-1 pour une liaison -OH libre
Pic plus large et plus arrondis entre 3200 et 3600 cm-1 pour une liaison -OH intermoléculaire (ex: les alcools)
Pic plus large et dentelé à la base entre 2500 et 3200 cm-1 pour une liaison -OH intramoléculaire
Groupement -NH2 et -NH
Pour -NH2,on a 2 bandes fine accolées entre 3100 et 3500 cm-1
Pour -NH, on a une bande fine entre 3100 et 3500
Groupement C=
On a une bande d'absorption forte entre 1600 et 1800 cm-1
Liaisons entre atomes de carbone
Les bandes des doubles liaisons C=C sont repérables entre 1620 et 1690 cm-1
Les bandes des triples liaisons C≡C sont repérables entre 2100 et 2260 cm-1
On observe 2 ou 3 bandes d'absorptions de moyenne intensité entre 1450 et 1600 cm-1, elles correspondent aux vibrations de valence C=C aromatique
Spectroscopie RMN (Résonance Magnétique Nucléaire)
Grâce à la spectroscopie RMN, on peut identifier des noyaux d'atomes comme celui de l'hydrogène ou du carbone
Cette technique est très efficace avec les molécules organiques car l'hydrogène est très présent
Principe
Un noyau d'hydrogène soumis à un champ magnétique se comporte comme un aimant
➥Il s'oriente parallèlement ou anti parallèlement au champ magnétique qu'il subit
On nomme ces deux états α et β
A chacun de ces deux états correspond un niveau d'énergie différent
Quand on irradie un échantillon avec une lumière dont la fréquence est telle que ΔE = hf, Tous les noyaux se mettent dans l'orientation β (la plus haute en énergie)
Comme les hydrogènes sont déjà soumis à un champ magnétique local, qui change selon l'environnement des noyaux
On dit qu'un noyau est blindé quand le champ magnétique local est faible
On dit qu'un noyau est déblindé quand le champ magnétique local est important
Déplacement chimique
Les variations de champ magnétique local créent une variation de la fréquence de résonance
➥Variation sur une gamme d'environ 900 Hz
On choisit un étalon interne (ex: (CH3)4Si) dont les 12 protons équivalents sont fortement blindés par rapport aux protons classiques
Ensuite, on définit le déplacement chimique par rapport à cet étalon
δ(ppm) = ${\text"distance du pic par rapport à la référence TMS(en Hz)"}/{\text "fréquence du spectrophotomètre (en MHz)"}$
REMARQUE: Les atomes très électronégatifs (F,O,Cl,Br) on un fort effet de déblindage sur les protons adjacents
L'intégration
Plus il y a de noyaux d'hydrogène d'un type donné dans la molécule, plus l'absorption RMN correspondante est forte
Pour connaître le rapport des noyaux, on mesure l'aire d'un pic et on la compare à la somme des aires des autres pics
On peut rajouter une courbe d'intégration au dessus des pics, la hauteur est proportionnelle au nombre de noyaux concernés
Règle N+1
Quand un groupe d'hydrogène est isolé d'un autre groupe, il est caractérisé par un pic que l'on nomme singulet
Si ce groupe est voisin d'un atome qui porte des hydrogènes, un couplage apparaît
➥Ce qui complique le spectre, on a donc la règle du N+1:
Pour On a N+1 pics pour N hydrogènes voisins
| Nombre d'H voisins équivalents | Nombre de pics (N+1) | Nom du profil des pics |
|---|---|---|
| 0 | 1 | singulet |
| 1 | 2 | doublet |
| 2 | 3 | triplet |
| 3 | 4 | quadruplet |
REMARQUE: on a 1 seul pic pour les H aromatiques
-
Partagez ce cours !
Suivez Nicolas KRITTER sur google + ( cours inspiré de celui fait par le professeur de la classe)